Понятие об ОВР и степени окисления. Понятие об окислителях, восстановителях, процессы окисления – восстановления. Типы ОВР. Окислительно – восстановительные свойства веществ. Способы нахождения коэффициентов. Установление возможности осуществления ОВР и изменения направления.
Химические реакции, протекающие с изменением степени окисления элементов, входящих в состав реагирующих веществ, называются окислительно – восстановительными (ОВР). В этих реакциях происходит обмен электронами, в них могут принимать участие твердые вещества, газы и жидкости.
Степень окисления – это условный заряд атома в соединении, вычисленный исходя из предположения о том, что все связи в атоме ионные.
Для определения степени окисления атомов в соединениях можно руководствоваться следующими положениями:
1) в простых веществах, например, Cl2, H2, N2, O2, Cu, Fe, Na и т.д. степени окисления атомов равны нулю;
2) степени кислорода во всех соединениях (-2), т.к. имея 2 непарных «холостых» электрона, кислород может образовать 2 ковалентные связи. Исключение:
Na2O2, H2O2 – пероксиды
степень окисления кислорода (-1) и соединение с фтором OF2 , степень окисления кислорода (+2), т.к. F будет более электроотрицательным элементом;
3) степень окисления водорода практически везде (+1), кроме гидридов NaH, СaH2 и т.д., где степень окисления Н (-1);
4) у некоторых элементов, характеризующихся постоянной валентностью будет постоянная степень окисления. Например, элементы IA группы (Li, Na, K, Rb, Cs, Fr) имеют степень окисления (+); элементы IIA группы (Be, Mg, Ca, Ba, Ra, Sr) – (+2); Al – (+3); Zn (+2); Cd (+2).
5) Алгебраическая сумма степеней окисления всех атомов, входящих в молекулу, равна нулю, т.к. молекула нейтральна. Это позволяет легко найти степень окисления любого элемента, как х.
правило (5) справедливо для ионов:
Иногда могут быть получены дробные или значения степени окисления, превышающие значение max. степени окисления.
Для этого составляются сначала графические или структурные формулы вещества.
У двух атомов S (+4), а у двух – (+1) (перекисная цепочка)
Сера имеет степень окисления (+6).
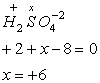






Комментариев нет:
Отправить комментарий