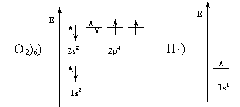 Представление о направленности ковалентных связей позволяет объяснить взаимное расположение атомов в многоатомных молекулах. Например, при образовании воды Н2О электронные облака двух атомов водорода (s) в форме шара перекрываются с двумя неспаренными р-электронами.
Представление о направленности ковалентных связей позволяет объяснить взаимное расположение атомов в многоатомных молекулах. Например, при образовании воды Н2О электронные облака двух атомов водорода (s) в форме шара перекрываются с двумя неспаренными р-электронами.
 |
Поскольку р-электроны ориентированы во взаимно перпендикулярных направлениях, то молекула Н2О имеет угловое строение, угол между связи д.б. 90˚. См. также молекулу NH3. Она построена в форме пирамиды. Углы между связями или как их называют валентные углы = не 90˚; в молекуле воды угол НОН=104,5˚, а в аммиаке HNH=107,3˚, т.е. тому состоянию молекулы, которому соответствуют наименьшая потенциальная энергия, и образуется более прочная ковалентная связь.
Комментариев нет:
Отправить комментарий